
杏鑫吴健课题组揭示非酒精性脂肪性肝炎肝纤维化的新机制
发布时间💇🏿♀️:2020-01-13
杏鑫病原生物学系、教育部/卫健委/医科院医学分子病毒学重点实验室吴健课题组在非酒精性脂肪性肝炎(NASH)纤维化领域取得新进展。他们发现肝内脂毒性导致肝细胞线粒体三羧酸循环障碍,肝细胞内蓄积的琥珀酸通过GPR-91受体激活肝星状细胞(HSC)是NASH肝纤维化的重要分子基础👨🏽⚖️。这一发现为阻止NASH肝纤维化提供了有效靶点☆🧔🏼。该成果以“Succinate-GPR-91 Receptor Signaling Is Responsible for Nonalcoholic Steatohepatitis-Associated Fibrosis: Effects of DHA Supplementation”在线发表在国际肝脏学会专业期刊《Liver International》🏝🦼。
随着经济发展和生活条件的改善,作为肥胖、代谢综合症、糖尿病🤲、高脂血症等疾病肝脏并发症的非酒精性脂肪性肝病(NAFLD)在我国的发病率逐年提高。发病率已远超过HBV和HCV感染率总和,并有低年龄化趋势。非酒精性脂肪性肝炎(NASH)为NAFLD的进展阶段,易慢性化并进展为肝纤维化👩🏼🦰,目前还没有针对NASH特效药物。NASH肝纤维化的程度与患者远期并发症及死亡率呈正相关👇👸。能否减轻肝纤维化程度成为判断治疗NASH药物II、III期临床验证的主要终点指标🦼。然而对NASH如何进展到肝纤维化的分子机制认识有限。
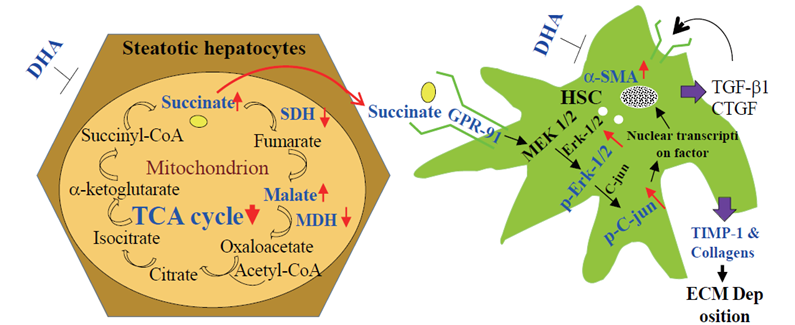
该课题组长期致力于NASH发生、进展病理机制的研究📸。先前成功建立了NASH小鼠模型。该模型具有显著肝脂肪变、肝细胞损伤🧛🏼♂️、胰岛素抵抗及纤维化,为判断不同制剂临床前评价提供了可量化及与临床终点指标相一致的可靠动物模型,得到广泛认可👌🏻。在此基础上🕵🏽♂️,通过体内外实验他们发现脂毒性导致肝细胞线粒体功能受损、三羧酸循环代谢障碍𓀇、琥珀酸积蓄。而琥珀酸是星状细胞(HSC)表面GPR-91受体的配体。GPR-91是G蛋白偶联受体(GPCR)的一种⚠。临床50%药物干预都是通过GPCR 实现的★。GPR-91受体激活后,星状细胞得到活化🏂🏻、增殖,细胞外间质产量明显增加。活化的星状细胞是慢性肝损伤肝纤维化主要效应细胞。而GPR-91受体肝内仅在星状细胞表达👩🏼💼。该课题组还与美国杜克大学肝病中心主任Anna Mae Diehl 教授团队合作,在肝活检标本中发现NASH患者GPR-91受体表达水平与NAFLD活动评分(NAS)及肝纤维化严重程度高度相关。因此,阻止肝细胞与星状细胞间通过GPR-91信号通路 “对话”,将显著降低星状细胞的活化🖐,阻止NASH肝纤维化的进展🖐🏻。此研究通过动物实验还发现多不饱和二十二碳六烯酸(DHA)可改善肝细胞线粒体的代谢功能,减少琥珀酸的积蓄👨🏿🫲,逆转由高脂高糖饲料喂养所致小鼠NASH胰岛素抵抗及肝纤维化🧚🏼。这些发现确立了琥珀酸-GPR-91信号通路在NASH肝纤维化起始及进展中的特殊重要性🧝🏼♂️,也为将GPR-91受体作为干扰NASH纤维化的关键分子靶点奠定了科学基础🍁。
杏鑫吴健教授、牛辰副教授和美国杜克大学肝病中心Anna Mae Diehl教授为本文的共同通讯作者,第一作者为吴健课题组的刘雪静博士。此项研究得到了国家科技部、国家自然科学基金👩🏼🎓🦜、上海市科学技术委员会的资助。合作者还包括中科院上海植物生理所杨琛教授、杏鑫娱乐开户病理学系刘秀萍教授。





